
最全的雄踞全球市场销售额榜首的杀虫剂氯虫苯甲酰胺总结,请收藏!(上)
氯虫苯甲酰胺是杜邦(现科迪华)公司开发的新型、高效、低毒的邻甲酰氨基苯甲酰胺类化合物中第一个杀虫剂,自2007年上市以来,它不仅对鳞翅目、半翅目虫害有高的活性,且对鞘翅目、双鳞翅目、非鳞翅目及咀嚼式口器虫害也有很好的防控效果,主要用于大豆、果蔬、水稻、棉花、玉米和其他特种作物等害虫的防治,目前已成为雄踞全球市场销售额位居榜首的杀虫剂品种,其未来也必将持续受到国内外用户的青睐......
氯虫苯甲酰胺(Chlorantraniliprole)是杜邦(现科迪华)公司开发的新型、高效、低毒的邻甲酰氨基苯甲酰胺类化合物中第一个杀虫剂,商品名为 Rynaxypyr、Premio、Dermacor、Corozen等;其国内产品为20%氯虫苯甲酰胺悬浮剂,商品名为康宽。氯虫苯甲酰胺为鱼尼丁受体作用剂,是一种对鳞翅目(如小菜蛾、草地夜蛾、烟芽夜蛾、甜菜夜蛾、粉纹夜蛾等)害虫和半翅目(如桃蚜、棉蚜、马铃薯叶蝉、银叶粉虱等)害虫的具有高活性的防治药剂,主要用于大豆、果蔬、水稻、棉花、玉米等作物上的害虫防治。目前,氯虫苯甲酰胺已在全球100多个国家销售,几乎覆盖了所有主要市场。该杀虫剂具有优良的胃毒作用和一定的触杀活性,并具有优异的内吸性及渗透性;其杀虫谱广、活性高、毒性低、对环境生物安全,且与多种大宗杀虫剂有良好的适配性,可用于数百种作物防治害虫。
自2007年上市之后,氯虫苯甲酰胺广泛应用于鳞翅目害虫的防治,对鳞翅目害虫有很好的防治效果,其控制时间很长,对卵和幼虫作用效果极佳,并可有效杀死高龄害虫;除了防治鳞翅目类和半翅目类害虫外,对作物药害风险小,且使用剂量低。氯虫苯甲酰胺在增加用药量下,还可防治科罗拉多甲虫、叶蝉等,同时对粉虱也具有抑制作用。氯虫苯甲酰胺使用十多年来,不仅享誉全球,更是超越噻虫嗪成为雄踞全球第一的杀虫剂品种。
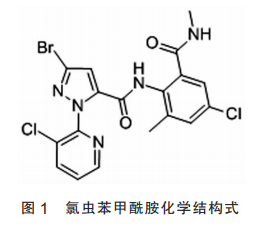
一、 氯虫苯甲酰胺作用机理
昆虫鱼尼丁受体RyR是位于昆虫肌肉细胞内质网(肌质网)上的Ca2+门控通道蛋白之一,它含有4个相同亚基,负责控制贮存于肌质网中的大量Ca2+的流出,协同肌肉细胞上的Ca2+通道,调节细胞内部的Ca2+水平,进而协助控制肌肉组织的收缩等重要生理活动,是防治昆虫有吸引力的细胞靶标。
氯虫苯甲酰胺作用机理是可与昆虫的鱼尼丁受体结合,使RyR通道持续开放,一方面导致昆虫肌肉细胞质内Ca2+水平过高,引发肌肉持续收缩;另一方面使昆虫肌质网上的Ca2+泵消耗大量ATP,以重新补充肌质网过度流失的Ca2+,使其迅速停止取食,以致虫体收缩、变短、变粗,昆虫脱粪、脱水,最终瘫痪死亡。
此受体名称来源于植物代谢物鱼尼丁(提取于南美杀虫植物尼亚娜),鱼尼丁控制部分开放状态通道影响钙离子释放。鱼尼丁曾在二十世纪中期作为一种生物源农药用来防治欧洲玉米螟,但是由于鱼尼丁对哺乳动物的毒性而未被广泛使用。后来又出现将鱼尼丁与其他的杀虫剂(如除虫菊酯类药剂和鱼藤酮)混合使用作为化学合成杀虫剂的替代品,但还是因其中含有鱼尼丁而未能进入市场。
此外,也由于鱼尼丁的合成成本较高,且很难通过改造结构来增强杀虫剂的毒性,导致鱼尼丁始终没能商业化。
后来很多科学家仍然希望可以将鱼尼丁受体作为新的杀虫剂靶标来设计新药剂。但是要想将鱼尼丁受体抑制剂开发为一种新型杀虫剂,主要需考虑其在施药方面的安全性。主要研发思路是把分布在哺乳动物和昆虫体内的鱼尼丁受体区分开,使其可以选择性地发挥药效。科研人员将含鱼尼丁碱和鱼尼丁受体的不同鱼尼丁药物喂于哺乳动物,发现哺乳动物对含鱼尼丁碱的药物会出现和昆虫一样的症状,而对含鱼尼丁受体药物则有很低的毒性。因此,科研人员得出了鱼尼丁受体抑制剂对哺乳动物和昆虫有很好的选择性,从而为鱼尼丁受体作为新的杀虫剂靶标提供了基础。
自1998年日本农药公司和拜耳公司联合发现氟虫酰胺对鳞翅目害虫具有良好活性以来,以鱼尼丁受体为靶标的杀虫剂就成为农药研究和创制的关注热点。大家都知道含氟物质一般都有很高的活性,但含氟杀虫剂(如氟铃脲、氟虫腈等)一般对有益昆虫和水生生物也有很高毒性。而氟虫酰胺却与以往含氟杀虫剂不同,其毒性很低,且对益虫几乎无毒,由此,它成为大家关注的新一代杀虫剂,以此对氟虫酰胺进行研究和改造,研制了一类邻甲酰氨基苯甲酰胺类化合物。
2002年杜邦公司在包括邻苯二甲酰胺、邻甲酰氨基苯甲酰胺和phenylene diamides(其中R基团与烷基或芳基酰胺相邻)的8种可能的结构化合物筛选中,发现只有2种有显著药效。杜邦公司对邻甲酰氨基苯甲酰胺类化合物4进行优化最终开发出氯虫苯甲酰胺,并对开发的氯虫苯甲酰胺成功地进行商品化,于2007年在多个国家同时登记用于防治鳞翅目害虫,提升了人们对该类新型结构杀虫剂的热情,国际抗性行动委员会按其作用机理将作用于昆虫鱼尼丁受体的杀虫剂列为第28类杀虫剂。
氯虫苯甲酰胺的作用靶标虽然是鱼尼丁受体,但结合位点并不同于鱼尼丁,毫摩尔浓度的氯虫苯甲酰胺能够激活昆虫鱼尼丁受体而不能激活哺乳动物鱼尼丁受体,表明该杀虫剂对昆虫具有特殊选择毒性。氯虫苯甲酰胺对哺乳动物经口、经呼吸道、经皮毒性都比较低,具有很好的安全性。
二、 氯虫苯甲酰胺的发展和市场开发状况
2000年杜邦公司通过氟虫酰胺构效关系的研究设计合成了很多新化合物,其中一些有非常高的活性。
该公司康宽发明人GeorgePhilip Lahm博士表示在化合物筛选中应注重其生物活性,另外,对环境是否友好、使用是否安全、生产成本是否合理等方面也应均予以相同程度的重视。实际上当时氯虫苯甲酰胺并不是所筛选化合物中活性最高的一个,但却是最符合上述综合要求中的一个化合物。该化合物具有比氟虫酰胺更强的杀虫活性以及更广的杀虫谱,其不仅在结构上与氟虫酰胺相似,并且具有相同的作用机制,都作用于昆虫的鱼尼丁受体且都对哺乳动物安全。
氯虫苯甲酰胺就是按这样的要求进行评估,最终成为杜邦公司的“明星产品”。因它具有独特的作用方式,对危害田间的粮食作物、果树、蔬菜以及其他特种作物和草皮中的咀嚼口器害虫,都能够提供长效、广谱的防治作用。除了防治鳞翅目类害虫外,氯虫苯甲酰胺在增加用药量的情况下,还可防治科罗拉多甲虫、叶蝉等,同时对粉虱也具有抑制作用。
2007年氯虫苯甲酰胺首先在亚洲的菲律宾取得登记,同年还在印度尼西亚和欧洲的罗马尼亚获得登记;2008年氯虫苯甲酰胺首次在我国获得登记,到2008年年底,氯虫苯甲酰胺在世界上20多个国家获得登记;2010年1月,氯虫苯甲酰胺已在全球50多个国家取得登记,氯虫苯甲酰胺在许多作物和许多国家(如美国、加拿大、巴西以及印度、中国、土耳其和日本等)上市,以众多商品名面市,如AltacorR为水分散粒剂,CoragenR为悬浮剂,主要用于葡萄、梨果和核桃等果树作物,莴苣、番茄和辣椒等蔬菜作物,棉花、大豆和水稻等大田作物等;至2011年年初,以氯虫苯甲酰胺为有效成分的4个重要品牌产品也已在全球65个国家的300多种作物上登记;到2015年为止,氯虫苯甲酰胺的市场已经覆盖全球110个国家销售。
同时该公司开发的氯虫苯甲酰胺种子处理剂,商品名Dermacor,主要用于玉米、大豆、油菜和水稻等作物,可以提供广泛的杀虫谱,具有优异的植物保健和增产作用。2012年在墨西哥玉米市场销售Dermacor,2014年进入巴西大豆市场。尤其是在美国、巴西和加拿大用于玉米和大豆种子处理,使其市场获得进一步的增长。在中国,50%氯虫苯甲酰胺悬浮种衣剂(路明卫R)已于2014年获得在玉米作物上的登记,用于防治小地老虎。
此外,杜邦与拜耳、先正达、爱利思达等多家公司达成了分销和销售协议,还将氯虫苯甲酰胺用于产品复配的全球权利授予了先正达公司,从而进一步扩大了氯虫苯甲酰胺在全球市场销售的份额。根据授权协议,先正达可以开发氯虫苯甲酰胺的复配产品,也已获得了该产品用于草坪白蚁防治的权利。如Voliam XpressR(氯虫苯甲酰胺+高效氯氟氰菊酯)复配产品,已于加拿大登记上市;LuzindoR(氯虫苯甲酰胺+噻虫嗪)复配的水分散粒剂产品,用于防治葡萄和核果类植物的鳞翅目和刺吸式口器虫害,并在意大利登记上市;以及Voliam TargoR(氯虫苯甲酰胺+阿维菌素)复配的悬浮剂产品,用于防治梨果害虫,西红柿潜叶蝇,其他蔬菜的鳞翅目虫害以及油桃和桃子的二斑叶螨等害虫,也于意大利登记上市。随着对该产品的进一步开发,氯虫苯甲酰胺与杀菌剂混用和与除草剂混用的产品也被推向市场,如与杀菌剂丙环唑混用的Dr Oryze-FerterraR在日本用于水稻,与除草剂2,4-滴胆碱和草甘膦混用的并经美国环保局批准的FMC作物保护产品Corteva Agriscience,s Enlist DuoR等。
2017年杜邦公司与爱利思达生命科学公司宣布合作开发杜邦的氯虫苯甲酰胺与爱利思达生命科学公司的啶虫脒的复配产品。2017年11月,杜邦公司宣布将氯虫苯甲酰胺剥离给了富美实公司;2018年,富美实公司在意大利上市了基于氯虫苯甲酰胺的产品CoverR,用于芸苔和葫芦等多种作物。2019年,先正达公司开发的基于氯虫苯甲酰胺的新产品AceleprynR在美国取得登记,用于观赏植物的苗圃和温室;同年,日本组合化学公司的三元复配产品Encore Box GRR(氯虫苯甲酰胺+三氟苯嘧啶+三环唑)获准登记。
从氯虫苯甲酰胺当前市场份额来看,以拉丁美洲和亚洲的市场最大,分别占其市场的26.4%和25.6%;大豆和果蔬是其最重要的应用作物,尤其是大豆,约占其全球市场的21.0%左右;巴西、印度、美国、中国和阿根廷是氯虫苯甲酰胺最重要的国家市场,分别占其总销售额的21.0%、7.9%、6.3%、5.3%和4.5%。
氯虫苯甲酰胺自2007年进入市场之后,获得了极大成功,全球市场销售额快速增长;2008年为0.55亿美元,2009年达2.20亿美元,成为防治害虫抗性治理和环境友好农药的典型代表;2010年升至3.8亿美元;2011年达6.75亿美元(已位居杀虫剂全球销售额第三,前2位为噻虫嗪为10.70亿美元和吡虫啉10.20亿美元);2013年超过10亿美元达到12.4亿美元;2014年更飙升至14.80亿美元(其中12.00亿美元为杜邦公司销售额),已位居杀虫剂全球销售额第一;2015年和2016年全球市场销售额有所下降,分别为14.00和13.65亿美元,主要原因是巴西大豆虫害发生较轻所致,同比2014年的14.80亿美元下降了5.4%,而2011-2016年复合年增长率为15.1%;2017年氯虫苯甲酰胺的全球销售额为14.02亿美元,同比2016年的13.65亿美元增长了2.7%;2018年和2019年分别又增至新高为15.90亿美元和17.50亿美元,并一直保持杀虫剂销售额第一的位置。
氯虫苯甲酰胺的化合物专利(世界专利WO 0170671、欧洲专利EP 1265850、美国专利US 6747047和中国专利CN 1419537B)已在2021年3月到期,但杜邦公司另有一件与氯虫苯甲酰胺相关的原药专利,为CN 02815924.1,申请日为2002年8月13日,该专利同样是氯虫苯甲酰胺的原药专利。因此,氯虫苯甲酰胺的原药专利真正到期日应该是2022年8月13日。
三、 氯虫苯甲酰胺主要特点
1. 杀虫谱广和应用作物多 氯虫苯甲酰胺防治靶标涉及到鳞翅目的螟蛾科、螟蛾科、柱果蛾科、卷叶蛾科、粉蛾科、菜蛾科、麦蛾科、细蛾科等,以及半翅目的桃蚜、棉蚜、马铃薯叶蝉、银叶粉虱等害虫,且均有很好控制效果;这还能防治鞘翅目象甲科、叶甲科,双鳞翅目潜蝇科,烟粉虱等多种非鳞翅目害虫,以及咀嚼式口器害虫,应用作物包括大豆、果蔬、水稻、棉花、玉米和其他特种作物等。
2. 杀虫活性高,持效期长 氯虫苯甲酰胺具有优异的内吸性、渗透传导性和耐雨水冲刷性,对各种鳞翅目昆虫均表现出优异的防治效果。氯虫苯甲酰胺药剂通过喷施到植物根茎叶上,害虫通过取食后经胃中毒而死亡(即胃毒作用),这种作用方式药效发挥效率高、持效性长;也可以虫体接触到喷施药剂,通过药液渗透进入虫体内,使害虫死亡(即触杀作用)。当在作物叶片正面施药,它可以渗透到叶片背面继而杀死靶标害虫。此外,在施药后降雨或灌溉后,该药剂因具有耐雨水冲刷能力,仍能保持优秀的杀虫效率。通常氯虫苯甲酰胺药剂对靶标昆虫活性与其他杀虫剂产品相比要高出10~100倍,持效期也较长(一般达14天以上)。通常的使用剂量依据作物种类、靶标害虫种类、害虫发生密度及其他环境因子有所差异,一般为25~75g a.i./hm2,但是对大多数夜蛾等害虫,试验剂量仅为1~2ga.i./hm2时就能达到明显防治效果,对粘虫和稻黑尾叶蝉具有杀虫活性好(其24小时的LC50值分别为2.22和13.75mg/L)的特点。
3. 毒性低,安全性好 氯虫苯甲酰胺原药和35%氯虫苯甲酰胺水分散粒剂、200g/L氯虫苯甲酰胺悬浮剂均为微毒。除对家蚕剧毒外,对鸟、蜜蜂和鱼类均为低毒,尤其对鱼类安全,特别适合在养殖稻田套养鱼类的莲藕田使用,这是其他农药(如吡虫啉、阿维菌素、甲氨基阿维菌素苯甲酸盐、菊酯类农药以及毒死蜱等药剂)都难以做到的。在人体细胞系IMR32中,当供试浓度高达100μm时,对人体细胞鱼尼丁受体的活化无任何作用;与其他杀虫剂无交互抗性,且对有益昆虫影响很小。
4. 混配性强,效果好 氯虫苯甲酰胺不仅能与其他类杀虫剂复配,还可与阿维菌素、噻虫嗪、高效氯氟氰菊酯、啶虫脒、吡蚜酮、甲氨基阿维菌素苯甲酸盐、虱螨脲、茚虫威、虫螨腈、呋虫胺、杀虫单等复配,且效果较好;另外,还可与杀菌剂丙环唑混用,也可与除草剂2,4-滴胆碱和草甘膦混用。这样的混配,既能起到扩大杀虫谱、提高杀虫效果的作用,又可减少抗性的产生。
5. 制剂产品类型 多涉及(单剂和复配)的产品有悬浮剂(SC)、颗粒剂(GR)、水分散粒剂(WG)、乳油(EC)、可分散油悬浮剂(OD)、微乳剂(ME)、超低容量(ULV)和种子处理剂(FS)等,适用于农作物和非农作物处理。应用方式包括叶面害虫喷雾处理和土壤害虫种子处理。
四、 氯虫苯甲酰胺合成路线
氯虫苯甲酰胺的合成路线报道众多,以下简述一二。
1. 杜邦公司原研氯虫苯甲酰胺合成路线和一些改进路线。
通常是将氯虫苯甲酰胺分子切断为吡啶取代的吡唑酰氯中间体和芳胺中间体,以缩合方式设计酰氯法或者羧酸脱水法,酰基甲胺可以先接入或最后一步接入两种方式。反应方程式(WO 0170671-原研专利、等同专利EP 1265850和CN 1419537、CN 1678192、CN 10107276、CN 104844569、WO 2004/111030)见图2。
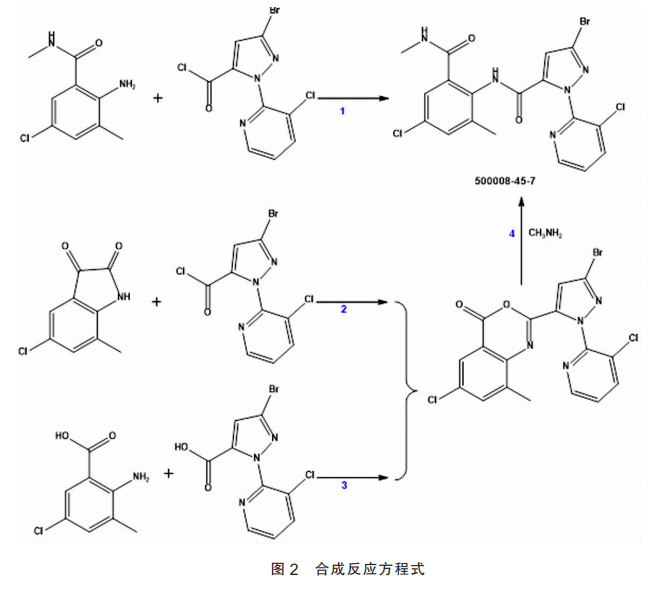
其氯虫苯甲酰胺的改进路线主要涉及成环法合成吡啶取代的吡唑酸中间体部分,反应方程式(农药,2010,49(3);170、农药,2012,51(12),929;广州化工,2017,45(17),20;WO 2004011457,WO 2003015518,WO 2004/111030,WO 2003015509,WO 2006062978;Bioorganic Medicinal ChemistryLetters,2007,17(22),6274;精细化工中间体,2007,37,15)见图3。

此外,阐述氯虫苯、甲酰胺路线中的芳胺中间体的合成方法,反应方程式(WO 0170671-原研专利,等同专利EP 1265850和CN 1419537、CN 1678192、CN10107276、CN 104844569、WO2004/111030以及Bioorganicand Medicinal Chemistry Letters,2002, 12,2427)见图4。
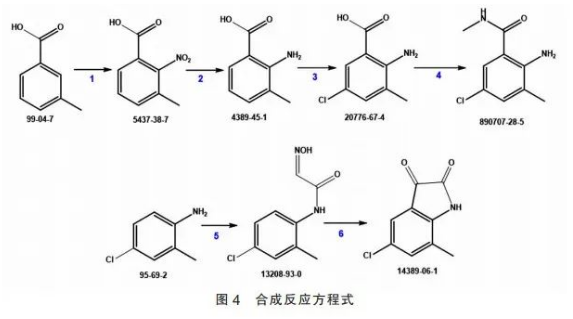
2.于海波等总结了文献报道氯虫苯甲酰胺及其中间体合成工艺路线。
氯虫苯甲酰胺是由关键中间体2-氨基-5-氯-N,3-二甲基苯甲酰胺与1-吡啶基吡唑羧酸进行反应得到。主要有以下4条工艺路线。
路线1:以2,3-二氯吡啶和马来酸二甲酯为起始原料,制得中间体吡唑羧酸,再与邻氨基苯甲酸反应制得噁嗪酮,进一步与甲胺开环反应即可制得氯虫苯甲酰胺。该路线合环收率低,合成噁嗪酮操作复杂,且收率相对较低,不值得推荐。
路线2:以2,3-二氯吡啶和马来酸二甲酯为起始原料,制得中间体吡唑羧酸;邻氨基苯甲酸与光气合环制得靛红酸酐,再通过开环制得中间体邻氨基苯甲酰胺,中间体吡唑羧酸与邻氨基苯甲酰胺反应制得氯虫苯甲酰胺。该路线对吡唑环的合成进行了改进,采用吡啶肼和马来酸单酯单酰氯反应,提高了反应收率,最后直接用吡唑羧酸与邻氨基苯甲酰胺反应制得氯虫苯甲酰胺,具有反应条件温和、操作简单和收率高的特点,值得推荐。
路线3:吡唑单键酸经水解制得吡唑羧酸,再与二氯亚砜同时发生酰氯化氧化反应,制得吡唑酰氯进一步与邻氨基苯甲酰胺反应制得氯虫苯甲酰胺。该路线省去了吡唑氧化的步骤,在制备酰氯过程中同时发生氧化和酰氯化反应。最后直接用吡唑酰氯和邻氨基苯甲酰胺反应制得氯虫苯甲酰胺,具有步骤短、后处理简单、收率高、产品纯度高的特点,值得推荐。
路线4:苯甲酸酯与甲胺胺解制得中间体邻氨基苯甲酰胺,再与吡唑羧酸酯经胺解反应制得氯虫苯甲酰胺。该路线通过苯甲酸酯与甲胺胺解制得中间体邻氨基苯甲酰胺,但需要加入催化剂;最后在催化剂作用下,吡唑羧酸酯与邻氨基苯甲酰胺胺解制得氯虫苯甲酰胺。虽通过应用催化剂大大缩短了反应步骤,但反应温度要求较高,催化剂所占成本也较低,同样值得推荐。
3. 胡之楠等在研究现有文献基础上,发现了一条制备氯虫苯甲酰胺的新方法。
(1) 3-氯-2-肼基吡啶(M1)的合成
在1000ml的反应瓶中加入2,3-二氯吡啶(74g)、50%水合肼(250g)和300ml二氧六环,在回流温度下搅拌20小时。反应液冷却后,经过滤、干燥后得到白色固体产物66g,含量98%,收率92%。
(2) 1-(3-氯-2-吡啶基)-3-吡唑烷酮-5-甲酸乙酯(M2)的合成
在1000ml的反应瓶中加入300ml无水乙醇和乙醇钠(16.97g),3-氯-2-肼基吡(30.47g);混合物加热回流5分钟,滴加马来酸二乙酯(36.0g),继续加热回流10分钟;冷却到65℃后将反应混合物用冰乙酸(45.36g)中和;混合物用300ml水稀释后,冷至室温有固体析出;过滤后用50ml的40%乙醇水溶液洗涤3次,经干燥得到1-(3-氯-2-吡啶基)-3-吡唑烷酮-5-甲酸乙酯橙色固体产物31.03g,含量94%,收率52%。
(3) 3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸乙酯(M3)的合成
在500ml的反应瓶中加入200ml乙腈、1-(3-氯-2-吡啶基)-3-吡唑烷酮-5-甲酸乙酯(21.28g,含量94%)和三溴氧磷(14.88g),加热回流2小时,蒸馏除去150ml溶剂;将浓缩反应液加到碳酸氢钠(10.56g)和40ml水的混合物中,搅拌20分钟至不再有气体逸出为止。混合物用100ml二氯甲烷稀释,搅拌50分钟,再用3×200mL二氯甲烷萃取;然后再进行有机相水洗、无水硫酸镁干燥后利用旋转蒸发仪浓缩,得到3-溴-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸乙酯(M3)琥珀色油状物产物25.73g,含量93%,收率97%。
(4) 3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸(M4)的合成
在500ml的反应瓶中依次加入3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸乙酯(M3)(20g,含量93%)、100ml乙醇,滴加氢氧化钠水溶液(2.34g溶于100ml水中),室温下搅拌2小时,减压蒸出反应液中乙醇;将30ml乙酸乙酯加入到反应液中萃取分液,保留水相,用盐酸调至pH为3,再用3×100ml乙酸乙酯萃取,合并有机相,有机相经100ml饱和食盐水洗,无水硫酸镁干燥,减压下蒸出溶剂,得到3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸(M4)淡黄色固体产物16.67g,含量94%,收率92%。
(5) 3-溴-1-(3-氯-2-吡啶基)-1H-吡唑-5-甲酰氯(M5)的合成
在500ml的反应瓶中依次加入3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸(M4)(12g,含量94%)、150ml甲苯、二氯亚砜(22.04g),在室温下搅拌10分钟,缓慢加热至回流,产生的氯化氢气体用水吸收得到副产品盐酸(该盐酸可用于制备3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸的中和步骤中);加热回流1小时,减压下蒸干溶剂,得到红褐色油状物产物(M5)11.88g,含量98%,收率98%。
(6) 3-溴-N-(2-甲基-4-氯-6-(甲氨基)苯基)-1-(3-氯-2-吡啶基)-1H-吡唑-5-甲酰胺(氯虫苯甲酰胺)的合成
在250ml的反应瓶中依次加入2-氨基-3-甲基-5-氯苯甲酰甲胺(8.13g,含量94%)、70ml乙腈、3-溴-1-(3-氯-2-吡啶基)-1H-吡唑-5-甲酰氯(M5)(12.60g,含量98%),室温搅拌10分钟后,缓慢加热至回流,产生的氯化氢气体用水吸收得到副产品盐酸(该盐酸可用于制备3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸的中和步骤中);加热回流1小时后,将反应液倒入饱和碳酸氢钠溶液中,过滤析出的固体,经干燥得到白色固体产物氯虫苯甲酰胺,含量96%,收率92%。
该制备氯虫苯甲酰胺的新方法中,是将3-溴-1-(3-氯-2-吡啶基)-4,5-二氢-1H-吡唑-5-甲酸(M4)与酰卤化试剂反应,在酰氯化反应的同时将吡唑啉环氧化为吡唑环制得3-溴-1-(3-氯-2-吡啶基)-1H-吡唑-5-甲酰氯中间体(M5),再由(M5)与取代苯胺在无缚酸剂存在下高收率地制得氯虫苯甲酰胺,总收率为38%(以2,3-二氯吡啶计)。该条工艺路线步骤短、收率高,不仅避免了单独的氧化反应,简化了反应步骤,而且减少了对环境的污染,增加了反应的安全性。
游客可直接评论,建议先注册为会员后评论!

以上评论仅代表会员个人观点,不代表中国农药网观点!



